فهرست عناوین
- آشنایی با استات ها و اهمیت آن ها
- ساختار شیمیایی یون استات
- رایج ترین ترکیبات استات و نام های متداول آن ها
- خصوصیات فیزیکی عمومی استات ها
- خواص اسیدی–بازی استات ها
- تولید صنعتی استات ها
- پایداری شیمیایی و عوامل تأثیرگذار بر آن
- تأثیر شکل فیزیکی استات ها در کاربردهای مختلف
- نقش استات ها در تنظیم PH و واکنش های شیمیایی
- مقایسه خواص فیزیکی استات ها با سایر نمک های کربوکسیلاتی
- کاربرد استات ها در صنایع غذایی و کشاورزی
- استفاده از استات ها در صنایع شیمیایی و دارویی
- ایمنی و ملاحظات نگهداری استات ها
نوشته شده توسط شرکت صنایع استات ایران
منتشر شده توسط شرکت صنایع استات ایران
تاریخ انتشار مقاله : 18-01-1404
تاریخ بروزرسانی مقاله : 18-01-1404
تعداد کلمات : 1500
آدرس مقاله : لینک مقاله
خواص فیزیکی و شیمیایی استات ها چیست

آشنایی با استات ها و اهمیت آن ها
استات ها نمک های اسید استیک هستند که فرمول عمومی آن ها CH₃COO⁻M⁺ است. M⁺ نشان دهنده کاتیون فلزی یا آمونیوم است. این ترکیبات در طبیعت به وفور یافت می شوند و نقش اساسی در بیوشیمی و بسیاری از فرآیندهای صنعتی ایفا می کنند. در ادامه نیز به تعریف استات و انواع آن خواهیم پرداخت. استات ها به طور گسترده در صنایع مختلف مانند تولید فیلم عکاسی ، مواد غذایی (به عنوان نگهدارنده) ، نساجی (به عنوان رنگرزی و پرداخت پارچه) و داروسازی کاربرد دارند. خواص فیزیکی و شیمیایی متنوع آن ها ، آن ها را به مواد اولیه ارزشمندی در سنتز ترکیبات آلی تبدیل کرده است. از جمله خواص مهم استات ها می توان به حلالیت بالا در آب ، قابلیت تشکیل کمپلکس با یون های فلزی و خاصیت بافری اشاره کرد.
ساختار شیمیایی یون استات
یون استات CH₃COO⁻ آنیون اسید استیک است. این یون از یک گروه متیل (CH₃) متصل به یک گروه کربوکسیلات (COO⁻) تشکیل شده است. گروه کربوکسیلات گروه عاملی اصلی استات ها است و دارای دو اتم اکسیژن است که یکی به کربن با پیوند دوگانه و دیگری با پیوند یگانه متصل شده است. بار منفی یون استات بر روی گروه کربوکسیلات متمرکز است و این تمرکز بار منفی سبب برهم کنش های الکترواستاتیکی و حلالیت بالای استات ها در آب می شود. ساختار مسطح و رزونانس در گروه کربوکسیلات ثبات یون استات را افزایش می دهد. این ساختار ساده و واکنش پذیری گروه کربوکسیلات سبب کاربرد وسیع استات ها در شیمی آلی و صنایع مختلف می شود.
| ردیف | ویژگی شیمیایی | تأثیر بار منفی روی کربوکسیلات | نوع برهمکنش | نتیجه در حلالیت | مثال استات مرتبط |
|---|---|---|---|---|---|
| 1 | پایداری یونی | افزایش پایداری رزنانسی | الکترواستاتیک قوی | حلالیت بالا | سدیم استات |
| 2 | قطبیت مولکول | تمرکز بار منفی در سر کربوکسیلات | جذب مولکولهای آب | محلول در آب | پتاسیم استات |
| 3 | پیوند هیدروژنی | تشدید قدرت گیرندگی الکترون | تشکیل پیوند هیدروژنی | افزایش انحلال | آمونیوم استات |
| 4 | رفتار اسیدی-بازی | کاهش خاصیت اسیدی | بازی ضعیف در محلول | محلول با pH خنثی | استات کلسیم |
| 5 | پایداری در محلول | تقویت دفع بین یونها | نیروی دافعه یونی | جلوگیری از تجمع | استات منیزیم |
| 6 | رفتار در محیط آبی | بار منفی باعث جذب قویتر آب | تشکیل پوسته آبی | انحلال سریع | استات لیتیم |
رایج ترین ترکیبات استات و نام های متداول آن ها
رایج ترین استات ها شامل استات سدیم NaOAc ، استات کلسیم Ca(OAc)₂ و استات آمونیوم NH₄OAc هستند. استات سدیم به عنوان نگهدارنده غذا و در کیسه های گرمایشی استفاده می شود. استات کلسیم در صنایع غذایی و به عنوان مکمل کلسیم یافت می شود. استات آمونیوم در بافرهای آزمایشگاهی و به عنوان حلال در شیمی آلی کاربرد دارد. دیگر استات های مهم شامل استات پتاسیم ، استات روی و استات مس هستند که کاربردهای تخصصی در صنایع مختلف دارند. نام های متداول اغلب به صورت اختصاری مانند NaOAc و NH4OAc نمایش داده می شوند.
خصوصیات فیزیکی عمومی استات ها
استات ها عموماً جامداتی بلوری و سفید رنگ هستند. نقطه ذوب و جوش آن ها به کاتیون متصل شده وابسته است. به طور کلی با افزایش وزن مولکولی ، نقطه ذوب افزایش می یابد. استات ها به طور کلی در آب بسیار محلول هستند اما حلالیت در حلال های آلی متفاوت است. استات های با کاتیون های کوچک تر مانند سدیم و آمونیوم حلالیت بیشتری در آب دارند. چگالی آن ها نیز به نوع کاتیون بستگی دارد. برخی استات ها مانند استات سدیم خاصیت هیگروسکوپیک دارند یعنی رطوبت هوا را جذب می کنند. ویژگی های ظاهری مانند رنگ و شکل بلورها نیز بین انواع مختلف استات ها متفاوت می باشد. البته همه استات ها به طور کلی مزه نمکی دارند.
خواص اسیدی–بازی استات ها
استات ها بازهای مزدوج اسید ضعیف استیک هستند. یون استات (CH₃COO⁻) می تواند با پذیرش پروتون (H⁺) از یک اسید یک مولکول اسید استیک تشکیل دهد. به همین دلیل است که استات ها معمولاً رفتار بازی ضعیف از خود نشان می دهند. واکنش استات ها با اسیدها واکنشی اسید-باز است که در آن اسید پروتون خود را به یون استات می دهد و اسید استیک و نمک مربوط به اسید مورد استفاده تشکیل می شود. قدرت بازی استات ها به نوع کاتیون متصل به آن بستگی دارد و با ثابت تفکیک بازی (Kb) کمیّت دهی می شود. Kb استات ها کم بوده که نشان دهنده رفتار بازی ضعیف آن ها است.
تولید صنعتی استات ها
تولید صنعتی استات ها عمدتاً از طریق دو روش اصلی انجام می شود : استیلاسیون و خنثیسازی. در استیلاسیون ، الکل ها با اسید استیک واکنش می دهند تا استرها تولید کنند که نوعی از استات ها هستند. این واکنش معمولاً با استفاده از کاتالیزورهای اسیدی انجام می شود. روش دوم خنثیسازی شامل واکنش اسید استیک با بازهای مختلف مانند هیدروکسید سدیم (NaOH) یا هیدروکسید آمونیوم (NH₄OH) است. این واکنش ها منجر به تولید استات های فلزی یا آمونیوم می شوند. انتخاب روش تولید به نوع استات مورد نظر و مقیاس تولید بستگی دارد. عوامل دیگری مانند خلوص مواد اولیه و هزینه ها نیز در انتخاب روش مؤثر هستند.
پایداری شیمیایی و عوامل تأثیرگذار بر آن
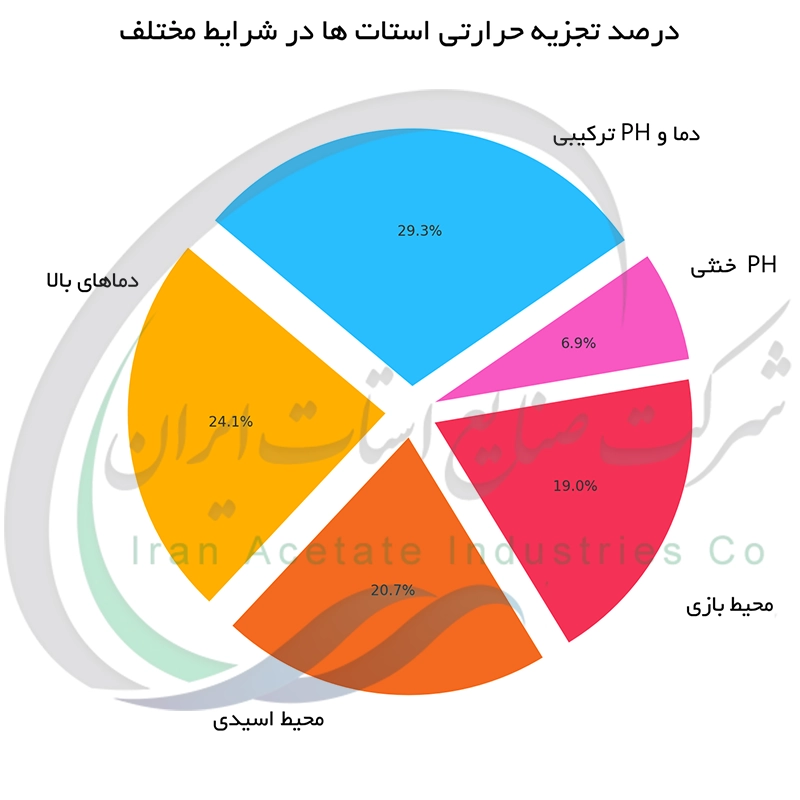
استات ها به طور کلی ترکیبات پایدار هستند اما پایداری آن ها تحت تأثیر عوامل محیطی قرار می گیرد. دماهای بالا می تواند به تجزیه حرارتی برخی استات ها منجر شود. PH محیط نیز اثرگذار است. در محیط های بسیار اسیدی یا بازی پایداری کاهش می یابد. رطوبت باعث هیدرولیز برخی استات ها به خصوص در حضور ناخالصی های کاتالیزوری می شود. وجود یون های فلزی خاص نیز واکنش های جانبی ایجاد کرده و پایداری را کاهش می دهد. بنابراین نگهداری استات ها در شرایط خشک ، دمای مناسب و PH خنثی برای حفظ پایداری آن ها الزامی است و آگاهی از این مورد برای نگهداری و خرید اتیل استات ضروری می باشد.
تأثیر شکل فیزیکی استات ها در کاربردهای مختلف
شکل فیزیکی استات ها (پودری ، کریستالی ، محلول) بر کاربردهای آن ها تأثیر مستقیم دارد. استات های پودری به راحتی در فرآیندهای اختلاط و پخش استفاده می شوند. استات های کریستالی برای کاربردهایی که نیاز به خلوص بالا و کنترل دقیق دارند مناسب ترند. محلول های استات ها در فرآیندهایی که نیاز به انحلال سریع و آماده سازی آسان دارند به کار می روند. مثلاً استات سدیم پودری در کیسه های گرمایی و استات های کریستالی در آزمایشگاه ها و استات های محلول در صنایع رنگرزی کاربرد دارند. انتخاب شکل فیزیکی به نیازهای خاص فرآیند و کاربرد بستگی دارد.
نقش استات ها در تنظیم PH و واکنش های شیمیایی
استات ها نمک های اسید ضعیف استیک ، در تنظیم PH محلول ها نقش حیاتی دارند. یون استات (CH₃COO⁻) می تواند با پذیرش یا آزادسازی پروتون (H⁺) در برابر تغییرات PH مقاومت کند. این ویژگی خاصیت بافری استات ها را نشان می دهد. به عنوان مثال محلول بافر استات سدیم/اسید استیک در محدوده PH 4 تا 5 ثابت می ماند و از تغییرات ناگهانی PH جلوگیری می کند. این بافرها در واکنش های حساس به PH مانند واکنش های آنزیمی و سنتزهای شیمیایی ضروری هستند. وجود یون استات در واکنش ها بر سرعت و بازده آنها نیز تأثیر می گذارد و در برخی موارد به عنوان کاتالیزور یا لیگاند عمل می کند.
مقایسه خواص فیزیکی استات ها با سایر نمک های کربوکسیلاتی
استات ها نمک های اسید استیک از نظر خواص فیزیکی با سایر کربوکسیلات ها مانند فرمات ها (نمک های اسید فرمیک) و پروپیونات ها (نمک های اسید پروپیونیک) شباهت هایی دارند. همه این ترکیبات در آب محلول بوده و نمک های کریستالی تشکیل می دهند. با این حال تفاوت هایی نیز وجود دارد. استات ها به دلیل گروه متیل (CH₃) دارای نقطه ذوب و جوش پایین تری نسبت به فرمات ها هستند. پروپیونات ها نیز نقطه ذوب و جوش بالاتری از استات ها دارند. حلالیت استات ها در حلال های آلی نیز با توجه به گروه جانبی متفاوت است. این تفاوت ها ناشی از تفاوت در اندازه و قطبیت گروه های آلکیل متصل به گروه کربوکسیلات است.
کاربرد استات ها در صنایع غذایی و کشاورزی
استات ها در صنایع غذایی به عنوان نگهدارنده ، طعم دهنده و تنظیم کننده PH کاربرد دارند. استات سدیم به عنوان نگهدارنده در محصولات فراوری شده و کنترل کننده ی اسیدیته در سس ها و ترشی ها عمل می کند. برخی استات ها طعم و مزه مطبوعی به غذا می بخشند. در کشاورزی استات ها به عنوان کودهای معدنی حاوی کاتیون های ضروری برای گیاهان مانند کلسیم و پتاسیم مورد استفاده قرار می گیرند. همچنین برخی استات ها در کنترل آفات و بیماری های گیاهی نقش دارند و به عنوان سموم دفع آفات ملایم به کار برده می شوند. اثرات مفید آن ها شامل افزایش جذب مواد مغذی و مقاومت گیاهان به استرس های محیطی می باشد.
استفاده از استات ها در صنایع شیمیایی و دارویی
استات ها در صنایع شیمیایی به عنوان حلال ، واکنش دهنده و واسطه در سنتزهای آلی کاربرد دارند. در تولید پلیمرها استات ها نقش مهمی در کنترل ویسکوزیته و بهبود خواص پلیمرها دارند. مثلاً سلولز استات در تولید فیلم و الیاف مصنوعی به کار می رود. در صنایع دارویی برخی استات ها به عنوان نمک های دارویی برای بهبود انحلال پذیری و جذب داروها استفاده می شوند. همچنین استات ها در فرمولاسیون برخی محصولات بهداشتی و آرایشی به عنوان تنظیم کننده PH و نگهدارنده حضور دارند . به عنوان مثال استات روی در برخی کرم های پوستی یافت می شود.
ایمنی و ملاحظات نگهداری استات ها
استات ها به طور کلی کم خطر هستند ولی ملاحظات ایمنی خاصی دارند. نگهداری آن ها در محیط خشک و خنک ، دور از منابع گرما و مواد ناسازگار ضروری است. از تماس مستقیم با پوست و چشم باید اجتناب شود. در صورت تماس باید بلافاصله با آب فراوان شستشو داده شود. حمل و نقل استات ها باید مطابق با قوانین مربوطه و با استفاده از بسته بندی مناسب انجام شود. استفاده از تجهیزات ایمنی فردی مانند دستکش ، عینک و ماسک در هنگام کار با استات ها توصیه می شود. در صورت بروز هرگونه حادثه باید به سرعت با مراکز درمانی تماس گرفته شود. اطلاعات ایمنی کامل را می توان در برگه های اطلاعات ایمنی (SDS) مربوط به هر استات خاص یافت.





واکنش های شیمیایی استات ها
خواص فیزیکی کلیدی استات ها
ساختار مولکولی استات ها